В своем земном или низком энергетическом состоянии углерод имеет два неспаренных электрона. Однако существует четыре полных внешних или валентных, электрона, то есть атомы углерода имеют четыре возможных участка склеивания.
В своем земном или низком энергетическом состоянии углерод имеет два неспаренных электрона. Однако существует четыре полных внешних или валентных, электрона, то есть атомы углерода имеют четыре возможных участка склеивания.
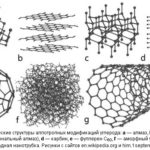
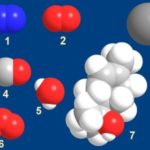
Из-за небольшого размера и четырех связующих участков углерод образует более различные типы соединений, чем любой другой элемент.
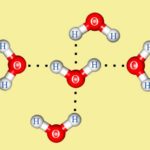
Это также единственный элемент, способный образовывать множество связей с другими атомами одного и того же типа. Углеродные связи могут быть одиночными, двойными, тройными или даже четверными, что означает, что углерод создает длинные цепи, а также кольца.
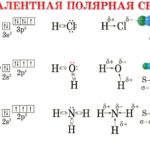
Большинство углеродных связей являются ковалентными, что означает, что все задействованные атомы разделяют электроны одинаково или неравномерно. Однако связь между углеродом и кальцием является ионной.