 Закон Гесса гласит, что полная энтальпия системы остается неизменной во время химической реакции, если указанная реакция состоит из одного шага или многих этапов. Это общая взаимосвязь в физической химии, которая описывает различия в реагентах и продуктах во всех химических реакциях. Закон Гесса был назван в честь Жермена Гесса, который опубликовал закон в 1840 году.
Закон Гесса гласит, что полная энтальпия системы остается неизменной во время химической реакции, если указанная реакция состоит из одного шага или многих этапов. Это общая взаимосвязь в физической химии, которая описывает различия в реагентах и продуктах во всех химических реакциях. Закон Гесса был назван в честь Жермена Гесса, который опубликовал закон в 1840 году.
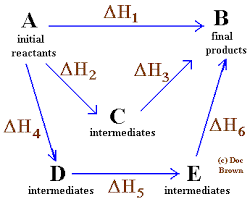
Закон Гесса также известен как закон постоянного теплового суммирования из-за закона, в котором утверждается, что сумма энтальпии каждой стадии реакции должна равняться поглощению или развитию тепла, даже если реакция протекает всего за один шаг. Из-за Закона Гесса студенты-химики могут аналитически найти полную энтальпию любой химической реакции.
Закон особенно полезен для расчета энтальпий реакций, которые трудно измерить химически из-за трудностей, которые трудно контролировать. Закон Гесса позволяет студентам и исследователям оценивать энтальпию реакций, добавляя все энтальпии образований для всех реагентов. Каждому обычному реагенту в химии была назначена энтальпия образования. Чтобы вычислить энтальпию реакции для любой химической реакции, необходимо добавить все энтальпии образования всех реагентов. Сумма энтальпий образования реагентов равна общей энтальпии реакции.